АЗ – аварийная защита.
аз – активная зона.
АР – автоматический регулятор.
АРМ – автоматический регулятор мощности.
АЧС – абсолютно чёрный стержень.
ББС – борно-бериллиевый стержень.
БКР – барометрический коэффициент реактивности.
БН – быстрые нейтроны.
БР – борное регулирование.
БРУ-СН (-К, - А) – быстродействующее редукционное устройство для сброса пара в конденсатор собственных нужд (в главный конденсатор, в атмосферу).
БС - бериллиевый стержень.
ВВРД – водо-водяной реактор с водой под давлением.
ВВРК – водо-водяной реактор кипящего типа.
ВВЭР – водо-водяной энергетический реактор.
ВКВ – верхний концевой выключатель (ОР СУЗ).
ВП – выгорающий поглотитель.
ВУГ – волновое уравнение Гельмгольца.
ГБС – гадолиний-бериллиевый стержень.
ГК – главный конденсатор.
ГУ – граничное условие (для получения частного решения дифференциального уравнения).
ГЦН – главный циркуляционный насос.
ДП – деаэратор подпитки.
ДУ – дифференциальное уравнение.
ДЭ – дифференциальная эффективность.
ЗН – замедляющиеся нейтроны.
ЗпН – запаздывающие нейтроны.
ЗР – запас реактивности.
ИЭ – интегральная эффективность.
ЙЯ – йодная яма.
КД – компенсатор давления.
КэВ – килоэлектронВольт.
МгН – мгновенные нейтроны.
МК – мгновенная критичность.
МКУМ – минимально контролируемый уровень мощности (реактора).
МН – медленные нейтроны.
МэВ – мегаэлектронВольт.
МЭР (МКР) – мощностной эффект (коэффициент) реактивности.
НКВ – нижний концевой выключатель (ОР СУЗ).
НП – нейтронное поле.
НУ – начальное (-ые) условие (-ия) для решения дифференциального уравнения.
НФИ – нейтронно-физические измерения.
НФХ – нейтронно-физическая характеристика.
НЦ – нейтронный цикл.
ОбЗР – общий запас реактивности.
ООСС – относительная обратная скорость счёта.
ОпЗР – оперативный запас реактивности.
ОР СУЗ – органы регулирования системы управления и защиты.
ПКУ – подкритический коэффициент умножения.
ПН – промежуточные нейтроны.
ПП – переходный процесс.
ПП – прометиевый провал.
ПТЭР (ПТКР) – плотностной температурный эффект (коэффициент) реактивности.
РБ – радиационная безопасность
РБМК – реактор большой мощности канальный
РзН – резонансные нейтроны.
РУ – резонансный уровень.
СВО – система специальной водоочистки.
СВП – самовыгорающий поглотитель.
СДУКР – система дифференциальных уравнений кинетики реактора (с учётом ЗпН).
СП – стержень-поглотитель.
СПУ – счётно-пусковая установка.
СЦРД – самоподдерживающаяся цепная реакция деления.
Т – абсолютная (выражаемая в Кельвинах) температура чего-либо.
t – температура чего-либо, выражаемая в градусах Цельсия.
ТВС – тепловыделяющая сборка.
твэл – тепловыделяющий элемент.
ТК – топливная композиция.
ТКР – температурный коэффициент реактивности.
Тн – температура тепловых нейтронов («нейтронного газа»).
ТН – тепловые нейтроны.
тн – теплоноситель.
ТТН – теплотехническая надежность (активной зоны).
ТЭР – температурный эффект реактивности.
УВФ – уравнение возраста Ферми.
УК – уравнение критичности реактора.
УОЧ – уравнение «обратных часов».
ФВ – физический вес (ОР СУЗ).
ЧС – чёрный стержень.
эВ - электронВольт
ЭВМ – электронная вычислительная машина.
ЭРИ – эффективный резонансный интеграл.
ЭУКР – элементарное уравнение кинетики реактора.
ЭЯР – энергетический ядерный реактор.
ЯБ – ядерная безопасность.
ЯИЗН – ядра-излучатели запаздывающих нейтронов.
ЯПЗН – ядра-предшественники запаздывающих нейтронов.
ЯР – ядерный реактор.
ЯТ – ядерное топливо.
ЯТЭР (ЯТКР) – ядерный температурный эффект (коэффициент) реактивности.
Тема 1.
ФИЗИЧЕСКИЕ ОСНОВЫ ПОЛУЧЕНИЯ ЯДЕРНОЙ ЭНЕРГИИ
1.1. Строение вещества
Все вещества состоят из молекул - частиц, каждая из которых определяет все физико-химические свойства вещества.
Молекулы простых веществ (К, Не, О2, Н2, Мо,...) состоят из одного или нескольких атомов одного химического элемента.
Молекулы сложных веществ (UO2, Н3ВО3, В4С, ...) состоят из атомов нескольких химических элементов.
Молекулы и составляющие их атомы различаются прежде всего по их массе. Для удобства сравнения массы различных молекул (атомов) принято измерять в относительных единицах, называемых атомными единицами массы (а. е.м.).
1 а. е.м. - это 1/12 часть массы изотопа атома углерода-12. В единицах системы СГС (которая чаще всего используется в нейтронно-физических расчетах) 1 а. е.м. эквивалентна 1.660567.10-24 г. Относительная масса молекулы или атома, выраженная в а. е.м., называется молекулярной (или атомной соответственно) массой и обозначается символом А.
Пространственную плотность молекул (атомов) в различных веществах принято оценивать величиной молекулярной (атомной) концентрации, то есть числом молекул (атомов), содержащихся в единице объёма вещества.
Опираясь на следствие закона Авогадро о том, что число молекул в 1 моле вещества - величина постоянная (называемая числом Авогадро NА = 6.0221.1023 моль-1), молекулярная концентрация любого вещества легко рассчитывается по известным величинам плотности g и молекулярной массы А вещества по формуле:
N = ![]() . (1.1)
. (1.1)
В единицах системы СГС размерность вычисленной по формуле (1.1) величины молекулярной концентрации – см -3, то есть молекул в 1 см3.
Таким образом, получается:
а) для простых веществ, каждая молекула которых содержит только один атом, молекулярная концентрация вещества по величине совпадает с атомной концентрацией и вычисляется по формуле (1.1);
б) для сложных веществ, каждая молекула которых содержит m сортов атомов различных химических элементов, молекулярная концентрация также находится по формуле (1.1), в которой молекулярная масса
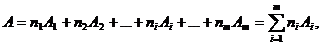 (1.2)
(1.2)
находимая по правилам химии, представляет собой сумму масс всех компонентов молекулы вещества; (здесь ni - число атомов каждого компонента в молекуле вещества, а Ai - атомная масса i-го компонента);
Пример. Кристаллическая борная кислота H3BO3 плотностью g = 1.28 г/см3 будет иметь относительную молекулярную массу:
А = 3Ан+1Ав+3Ао = 3. 1 + 1 .10.81 + 3 .16 = 61.81 а. е.м.,
а, следовательно, её молекулярная концентрация будет равна:
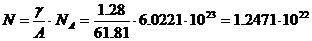 см-3.
см-3.
в) атомные концентрации компонентов сложных веществ находятся по общей формуле:
![]() (1. 3)
(1. 3)
где ni - число атомов i-го компонента в каждой молекуле вещества, а N - молекулярная концентрация вещества.
Пример.
В упомянутом выше примере борной кислоты:
- атомная концентрация водорода Nн= 3N = 3 .1.2471.1022 = 3.7413 .1022 см -3, т. к. в каждой молекуле борной кислоты содержится по три атома водорода;
- атомная концентрация бора Nв = N = 1.2471 .1022 см -3, т. к. в молекуле борной кислоты содержится только один атом бора;
- атомная концентрация кислорода No= 3N = 3 . 1.2471 .1022 = 3.7413 .1022 см -3, т. к. в каждой молекуле борной кислоты по три атома кислорода.
г) атомные концентрации в простых многоатомных веществах, очевидно, можно рассматривать как частность случая (в) и находить по общей формуле (1.3).
Пример. Молекула йода (J2) содержит по два атома химического элемента йода, поэтому атомная концентрация йода в кристаллическом йоде плотностью g = 4.9 г/см3 будет равна
![]()
1.2. Строение и характеристики атомов
Атомы различных химических элементов отличаются прежде всего по их массе, и атомная масса в какой-то мере определяет периодичность повторения химических свойств различных атомов. Однако массовое число A не является однозначной характеристикой всех свойств атомов любых веществ.
Действительной характеристикой, определяющей физико-химическую индивидуальность атома вещества, является его атомный номер (z) в открытой Периодической Системе элементов. Называя атомный номер элемента z, мы фактически называем сам этот элемент, об атомах которого идёт речь.
Например, если z = 6, нам ясно, что речь идет об углероде (С), а если z = 92, это равносильно тому, что элемент назван ураном (U), и т. д.
Поэтому атомный номер элемента z - характеристика, равноценная принятому химическому символу атомов вещества.
Массовое число A и атомный номер z элемента - пара характеристик, полностью определяющих физико-химическую индивидуальность атомов любого вещества.
Атомная теория раскрывает физический смысл этих характеристик
в следующих основных положениях:
а) Все атомы состоят из положительно заряженного ядра и обращающихся вокруг него отрицательно заряженных частиц - электронов.
б) Электрический заряд электрона qe = - 1.6022 .10-19 Кл - наименьший электрический заряд, обнаруженный экспериментально, и это дало повод назвать его элементарным зарядом, а заряды других частиц и структур на микроуровне - измерять в элементарных зарядах.
в) Атомный номер элемента z - есть не что иное, как суммарное количество электронов в атоме.
г) Поскольку устойчивый атом любого химического элемента электронейтрален, отрицательный заряд электронных оболочек в атоме нейтрализуется равным по величине положительным зарядом ядра. Поэтому другое представление об атомном номере состоит в том, что атомный номер химического элемента - это положительный заряд ядра его атома, выраженный в величинах элементарных электрических зарядов (то есть в зарядах электрона).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86 87 88 89 90 91 92 93 94 95 96 97 98 99 |



